本文为节选内容
如需更多报告,联系客服购买
可购买单份报告或打包(100多份医药健康报告,覆盖脑机接口、合成生物、生物医药、基因、中医药等)
CGT技术基础包括两大核心技术,即基因编辑技术和基因递送技术。
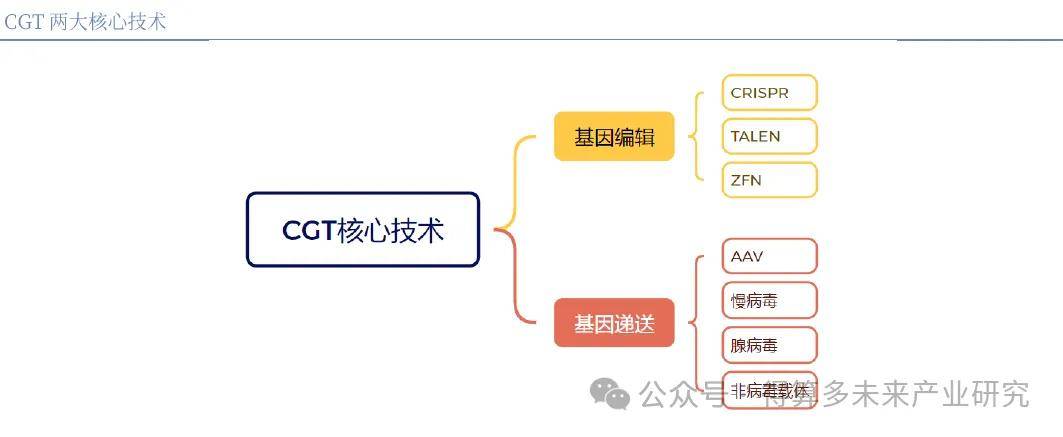
核心技术一一一基因编辑技术:基因编辑技术是一种能够对生物体基因组特定DNA序列进行精确修饰的技术,通过改变DNA序列来改变基因的功能,包括基因的表达、蛋白质产物的结构等诸多方面。可以利用基因编辑技术修正致病基因,治疗单基因遗传病,如镰状细胞贫血、囊性纤维化等,通过基因编辑可以精准地修复突变位点,恢复基因的正常功能。
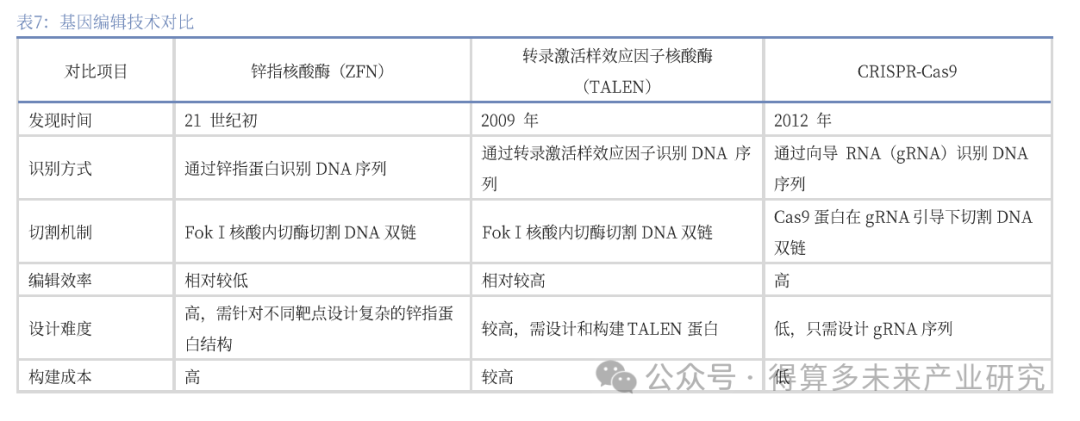
1.ZFNs:1983年锌指蛋白(Zinc finger protein,ZFP)首次在非洲爪蟾的转录因子IIA中被发现,第一种经过改造的人工核酸内切酶一一锌指核酸酶(Zincfingernueleases,ZFN)在20世纪90年代末首次得到研究和应用临床转化和开发一一第一代基因编辑技术ZFN技术发展于1996年,其目的基因特异性识别基于锌指蛋白,DNA切割依赖于FOkI核酸内切酶。每个锌指蛋白可识别并结合一个特异的三联体碱基,通过锌指蛋白的排列,可实现对DNA序列的靶向性。但是ZFN的研发成本相对较高,合成较为困难,涉及到蛋白筛选体系,因此技术开发和临床研究发展缓慢。
SangamoTherapeutics具有ZFN的数个关键专利,几乎垄断了ZFN技术的所有临床转化和开发。
2.TALEN:2007年植物黄单胞菌分泌的转录激活子样被发现,同理构建的转录激活因子样效应物核酸酶(Transcription activator-like effector nucleases,TALENs)脱靶几率小,细胞毒性小,成为另一种能够高效简便地靶向基因组的技术。TALEN技术发展于2011年,工作原理与ZFN基本类似,DNA切割同样依赖于FOkI核酸内切酶,但其目的基因特异性识别基于转录激活因子效应物,每两个氨基酸组合对应一个特定的碱基。TALEN的识别技术相比较于ZFN设计更加简便,操作更加灵活,但其高昂的研发费用一定程度上阻止了其发展。

3.CRISPR/Cas9:突破性的第三代基因编辑技术2012年,基于细菌获得性免疫系统的CRISPR/Cas9基因编辑技术出现并运用于哺乳动物中。CRISPR/Cas9的sgRNA可与基因组上特定序列结合,招募Cas9核酸内切酶并产生DNA双链断裂。作为目前最热门最强大的基因编辑系统,CRISPR/Cas9技术由于其简单快捷的设计和构建方法、低廉的成本和较低的脱靶效率,被迅速运用于各类疾病的细胞与基因治疗中,为其带来了革命性的突破,在临床上极具应用潜力。2016年,四川大学华西医院为国际上首个开展CRISPR/Cas9临床研究(NCT02793856)的机构,利用基因编辑技术在T细胞中敲除PD-1基因治疗非小细胞肺癌。2019年,EDIT-101被FDA批准用于Leber先天性黑蒙症10型的临床治疗研究中,这是第一个体内开展的CRISPR/Cas9临床试验。目前为止,在ClinicalTrials有超过30个基于CRISPR/Cas9的细胞与基因治疗临床试验注册,其中绝大多数为针对肿瘤的临床试验,也有针对血液和眼部疾病的临床试验。中国是目前为止基于CRISPR/Cas9技术开展临床试验最多的国家。
4.新型CRISPR/Cas9技术:近几年基因编辑技术不断创新,更迭迅速,除了传统的CRISPR/Cas9技术以外,一些新型的基于CRISPR/Cas9的基因编辑技术也逐步出现,包括CRISPRi,CRISPRa,碱基编辑器和引导编辑等。
核心技术二一一基因递送:基因递送技术是一类将外源基因(如治疗性基因、标记基因等)有效地运输到细胞内部的技术,这是CGT应用的关键步骤。载体主要包括病毒和非病毒载体,病毒载体递送效率高、具有组织特异性、可插入宿主基因组,在药物研发中被广泛使用,约60%-70%的CGT临床试验使用病毒载体。非病毒载体操作简单、成本小、免疫原性低,受到越来越多的关注,有望在将来替代病毒载体,降低细胞与基因治疗药物开发成本。
1.病毒载体介导的基因递送
1)腺病毒载体(AdV):腺病毒是一种无包膜的双链DNA病毒,其基因组大小约为36kb。腺病毒载体通过对野生型腺病毒进行改造而得,去除了病毒的部分非必需基因,插入外源基因,同时降低病毒的致病性。
腺病毒主要通过与细胞表面的受体(如柯萨奇-腺病毒受体,CAR)结合,然后通过受体-介导的内吞作用进入细胞。进入细胞后,病毒粒子在溶酶体中脱壳,释放出病毒基因组,进入细胞核并进行基因表达。腺病毒载体不会整合到宿主细胞基因组中,因此基因的表达是暂时的,可能需要反复给药来维持治疗效果。
应用领域:腺病毒载体在基因治疗领域应用广泛,尤其是在肿瘤治疗和疫苗开发方面。
2)腺相关病毒载体(AAV):腺相关病毒是一种单链DNA病毒,基因组较小,约为4.7kb。
腺相关病毒载体是一种复制缺陷型病毒,需要腺病毒或疱疹病毒等辅助病毒才能复制,因此其安全性高;同时他能在多种细胞类型中实现长期稳定的基因表达,免疫原性相对较低。
AAV通过与细胞表面的特定受体(如硫酸乙酰肝素蛋白聚糖等)结合,然后以内吞的方式进入细胞。进入细胞后,单链DNA基因组进入细胞核,在宿主细胞的帮助下转变为双链DNA,然后整合到宿主基因组(主要是在19号染色体的特定位置)或者以游离体的形式存在,从而实现基因表达。
应用领域:AAV载体在基因治疗领域,特别是对于一些遗传性疾病的治疗备受关注,主要用于眼部、大脑、肌肉和肝脏疾病的治疗中。
3)慢病毒载体(LV):慢病毒属于逆转录病毒家族,是一种有包膜的RNA病毒。其基因组为单链RNA,通过逆转录过程可将RNA转变为DNA后整合到宿主细胞基因组中。慢病毒载体是在野生型慢病毒的基础上改造而来,具有可以感染分裂和非分裂细胞的特性,能够携带较大的外源基因片段,一般可达8-10kb。
慢病毒主要通过与细胞表面的受体(如CD4和CCR5或CXCR4等)结合,包膜与细胞膜融合,病毒核心进入细胞。在细胞内,病毒RNA在逆转录酶的作用下转化为DNA,然后在整合酶的帮助下整合到宿主细胞基因组中,从而实现长期的基因表达。
目前行业普遍使用的是第三代慢病毒载体一一四质粒瞬时转染系统,即由1个包含目的基因的表达质粒GOI、2个包装质粒Rev和GagPol、1个包膜蛋白质粒VSV-G等4个质粒共转染HEK293细胞,整个生产工艺分为上游工艺(upstreamprocessing,USP)和下游工艺(downstreamprocessing,DSP)。USP主要是细胞培养和病毒包装,具体包括细胞复苏和扩增、细胞培养、四质粒瞬时转染。DSP主要是去除病毒收获液的杂质,提高纯度和滴度,保证载体的安全性和效率,具体包括收获澄清、DNA去除、层析、TFF、除菌过滤和灌装等环节。
应用领域:慢病毒载体在基因治疗和基因编辑领域应用广泛,可以将正常的造血干细胞基因递送至患者体内,重建正常的造血功能。
2.非病毒载体介导的基因递送
1)脂质体载体:脂质体是一种人工合成的脂质双分子层囊泡,其内部可以包裹水溶性的基因(如质粒DNA)。脂质体的组成成分主要是磷脂,通过调整磷脂的种类、比例和添加一些辅助成分(如胆固醇),可以改变脂质体的性质。脂质体载体具有良好的生物相容性,相对安全,并且可以通过修饰表面基团来增加其靶向性。
脂质体与细胞膜的融合是其主要的细胞进入方式。由于脂质体和细胞膜都具有脂质双分子层结构,它们可以在一定条件下融合,将包裹的基因释放到细胞内部。此外,脂质体也可以通过内吞作用进入细胞,然后在细胞内的溶酶体中释放基因。
应用领域:脂质体载体在基因治疗和药物递送方面有广泛的应用,脂质体可以包裹化疗药物和治疗性基因,实现联合治疗,同时减少药物对正常组织的副作用。
2)阳离子聚合物载体:阳离子聚合物是一类带有正电荷的聚合物,如聚乙二胺(PEI)等。它们可以通过静电相互作用与带有负电荷的基因(如DNA或RNA)结合,形成稳定的复合物。阳离子聚合物载体的优点是可以携带较大的基因片段,并且可以通过修饰来改善其物理化学性质和生物活性。
阳离子聚合物-基因复合物主要通过内吞作用进入细胞。进入细胞后,复合物需要从内吞泡中逃逸出来,以避免被溶酶体降解,然后将基因释放到细胞质或细胞核中。
应用领域:在基因治疗和基因编辑领域,阳离子聚合物载体可以用于递送各种基因材料。
3)无机纳米粒子载体:无机纳米粒子(如金纳米粒子、碳纳米管、量子点等)可以作为基因递送载体,具有良好的生物相容性和化学稳定性,可以通过表面修饰(如连接阳离子聚合物或靶向分子)来实现基因的有效结合和靶向递送。无机纳米粒子载体进入细胞的方式多种多样,包括内吞作用、与细胞膜的直接相互作用等。应用领域:可以利用纳米粒子的靶向性将治疗性基因递送至肿瘤细胞,实现精准治疗,同时利用纳米粒子的成像特性(如量子点的荧光特性)来监测治疗过程。